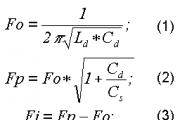Азотные удобрения: как и когда вносить в технологии Ноу-тилл? Доступные для растений формы азота Органические формы азота.
План.
- Содержание и формы азота в почве
- Процессы превращения азота в почве
- Некоторые особенности питания растений нитратным и аммиачным азотом
- Баланс азота почвы
- Содержание и формы фосфора.
- Доступность почвенных фосфатов растениям (условия, определяющие их растворимость).
- Баланс фосфора
- Содержание калия в почвах
- Формы и доступность почвенного калия растениям
- Баланс калия
Содержание азота в земной коре, по данным А.П. Виноградова, составляет 2,3*10 -2 весовых процента, а общие запасы исчисляются десятками млрдов. тонн. Основная часть азота почвы находится в виде сложных высокомолекулярных органических соединений. Некоторая часть азота земной коры находится в виде необменнопоглощенных ионов аммония и удерживается в кристаллической решетке алюмосиликатных минералов.
В пахотном слое разных почв количество азота колеблется в широких пределах; в дерново-подзолистых, песчаных и супесчаных почвах 0,04 0,08%, суглинистых и глинистых 0,1 0,15%. Серые лесные и черноземные почвы наиболее богаты общим азотом (0,3 0,5% и более). В каштановых почвах его количество колеблется от 0,1 (в светло-каштановых и бурых) до 0,2-0,25% (в темно-каштановых).
Азот в почвах находится преимущественно в недоступной растениям органической форме, минерального азота в них всего около 1% от общего. Под влиянием биологических процессов органический азот частично переходит в легкоусвояемые растениями минеральные формы. Распад азотных органических веществ почвы до аммиака (аммонификация) осуществляется аэробными и анаэробными микроорганизмами. Аммиак, накапливающийся в анаэробных условиях, поглощается почвенными коллоидами к может усваиваться растениями. В аэробных условиях аммиак под влиянием специфических микроорганизмов переходит в нитриты и затем окисляется до нитратов (нитрификация). Интенсивность минерализации органического вещества в разных почвах неодинакова, нитратный азот хорошо доступен растениям. Некоторое количество минерального азота поступает в почву с осадками. Атмосферный азот усваивается также отдельными микроорганизмами, живущими свободно, и клубеньковыми бактериями бобовых растений. Однако эта величина прихода азота в почву относительно невелика.
В почвах одновременно с минерализацией органических азотсодержащих веществ идет процесс перехода минеральных соединений азота в органические, недоступные растениям формы. Кроме того, содержание минерального азота в почве уменьшается а результате денитрификации, развивающейся в анаэробных условиях. При этом нитратный азот восстанавливается микроорганизмами до свободного газообразного азота, который теряется из почвы. Азот теряется также в результате вымывания нитратов, особенно из легких почв, осадками и дренажными водами.
Исследованиями ВИУА и Почвенным институтом имени В. В. Докучаева установлено, что 35 55% азота в зависимости от формы вносимого удобрения усваивается сельскохозяйственными культурами на дерново-подзолистых и серых лесных почвах, 25 45% закрепляется в почве и 0,1% теряется при вымывании, что не имеет существенного значения в азотном балансе тяжелосуглинистых почв. С помощью 15N установлено горизонтальное перемещение азота в почве и концентрация его в прикорневой зоне. Прогнозирование действия азотных удобрений на основе агрохимического анализа почв пока еще не дает ощутимых результатов. Соответствия между показателями отдельных методов и фактической прибавки урожаев не наблюдалось. Трудности в определении подвижного азота связаны с тем, что доступность его растениям определяют не только свойства самой почвы, но также погодные условия и агротехника. Обеспеченность растений азотом в значительной степени зависит от сезонной динамики процессов аммонификации и нитрификации, что может обусловить на одной и той же почве резкие различия в снабжении сельскохозяйственных культур этим элементом. Поэтому нет возможности дать характеристику почв по содержанию подвижного азота на основе данных массовых анализов, как по содержанию подвижных соединений фосфора и калия.
Преобладающая часть почвенного азота (95-98%) находится вместе с углеродом в составе органического вещества. Органический азот в почве, обладая достаточной устойчивостью, поддерживает ее плодородие, оставаясь недоступным растениям. В связи с этим немецкий ученый Шульц писал: «Если не говорить о воде, то именно азот является самым могучим двигателем в процессах развития, роста и творчества природы. Его уловить, им овладеть задача, его сберечь ключ к экономике, подчинить себе его источник, бьющий с неистощимой энергией тайна благосостояния».
Органический азот почв составляет основную долю азотного фонда пчв, представлен сложными разнообразными соединениями. Господствующая часть органического азота (82-89% от общего) входит в собственно гумусовые вещества. Остальная часть азота (3-11%) включена в состав неспецифических соединений (аминокислоты, аминосахара, битумы). В этой же группе находится азот негумифицированных органических веществ (ткани отмерших растений и животных, живая и мертвая масса микроорганизмов). В почвах от 200 до 300 кг/га азота включено в неспецифические органические вещества. Этот азот является основным резервным фондом для минерализации и накопления подвижных минеральных форм азота в процессе аммонификации и нитрификации.
В почвах элювиального ряда его содержание колеблется от 1,5 до 6 т/га, в серых лесных возрастает до 10,5 т/га, а в черноземах достигает 13,5-15 т/га. Трудно- и легкогидролизуемый азот образуется в результате неполного разложения органического материала почвы. Эта форма азота частично доступна для растительного организма. Следовательно, непрерывные циклы созидания и разрушения азотистых веществ приводят к накоплению в почве доступных растениям соединений азота. Основу превращений составляют процессы минерализации и иммобилизации.
Рис. Круговорот азота в природе
Минерализация означает превращение органического азота в минеральный посредством аммонификации и нитрификации. Таким образом, в почве формируются минеральные формы азота: аммонийная, нитритная, нитратная – они легко усваиваются растениями, на них приходится до 5% от общего азота. Начальным процессом минерализации органических соединений является аммонификация распад азотсодержащих органических соединений до аммонийного азота, органических кислот, углекислого газа. Аммонификация осуществляется в широком интервале рН, как в аэробных, так и в анаэробных условиях целым рядом микроорганизмов. Под воздействием протеолитических ферментов, выделяемых различными группами микроорганизмов, белковые вещества гидролизуются до аминокислот. Последние легко усваиваются микроорганизмами и под воздействием ферментов микробных клеток подвергаются процессам дезаминирования. В результате от амино - и амидосоединений отщепляется аммиак и образуются различные органические кислоты, углекислый газ, метан. Ежегодно в процессе аммонификации высвобождается до 2% азота от общих запасов азотсодержащих органических соединений. При этом, если соотношение С:N в субстрате узкое, происходит накопление аммонийного азота в почве, если широкое (солома, опилки), высвобождающийся аммоний тут же потребляется микроорганизмами для построения своего тела. Т. е. проявляется процесс иммобилизации азота трансформация микроорганизмами его минеральных форм в органические вещества микробных клеток и их метаболитов.
2. Процессы превращения азота в почве.
Какова судьба аммонийного азота почвы?
Предшественник, возделываемая культура, обработка почвы оказывают слабое влияние на накопление обменного аммония. Существенное влияние на режим обменного аммония оказывают гидротермические условия: при избыточном и недостаточном увлажнении и холодной погоде количество его возрастает.
1. Аммонийный азот легко вовлекается в процессы биологического поглощения, растения могут усваивать до 80% его запасов. Благоприятные условия для этого рН = 6, высокая концентрация ионов K, Ca, Mg.
2. При оптимальных значениях влажности и высокой поглотительной способности весь аммонийный азот по мере появления может удерживаться в почве в обменно-поглощенном состоянии (вовлекается в обменные процессы с почвенным поглощающим комплексом).
3. В определенных условиях возможно необменное поглощение аммонийного азота. При наличии минералов с трехслойным строением кристаллической решетки необменная фиксация может достигать до 5-21%. Присутствие K, Ca уменьшают, а смена условий увлажнения высушивания почв усиливает необменное поглощение аммонийного азота.
4.Большая часть аммонийного азота почвы окисляется до N-NO 3 , N-NO 2 , N-NO и N 2 . Это явление впервые открыл Луи Пастер в XIX веке и назвал нитрификацией. Она осуществляется группой специфических бактерий, для которых это окисление является источником энергии.
Нитрификация осуществляется в 2 этапа. В окислении аммиачных солей до нитритов: 2NH 3 + 3O 2 > 2HNO 2 +H 2 O, принимают участие бактерии родов: Nitrosomonas, Nitrosocystis, Nitrosospira, а до азотной: 2HNO 2 + O 2 > 2HNO 3 – бактериями рода Nitrobacter. Как видно, нитрификация – аэробный процесс, для ее интенсификации необходимы постоянный источник аммонийного азота и кислорода, оптимальные значения температуры – 20-25 0 С, влажности 60% от полной влагоемкости, рН = 6,2-8,2. Интенсивность минерализации органического вещества в разных типах почв неодинакова. В дерново-подзолистых почвах она протекает интенсивнее, чем на черноземах, где органическое вещество разлагается слабее. Ранней весной нитрификация осуществляется слабо, поскольку в почве содержится избыток влаги, почва слабо прогрета. По мере прогревания, нитрификация активизируется, ее пик приходится на конец июня - начало июля.
Наблюдения за содержанием нитратов в почвах показывает, что накопление этой формы минерального азота определяется потенциальными запасами почвенного плодородия. С повышением содержания гумуса и общего азота от дерново-подзолистых к серым лесным почвами далее к черноземам возрастает накопление нитратного азота. Наибольшей мобизизационной способностью обладают черноземы выщелоченные. В пахотном слое этих почв накапливается более 30 кг азота на гектар. В дерново-подзолистых почвах, несмотря на высокую относительную мобильность азотсодержащих органических соединений, образуется немного нитратов около 10 кг/га, поскольку общее количество гумуса и азота в них низкое.
Содержание нитратного азота во всех почвах четко определяется предшествующей культурой севооборота. Наиболее активно процессы нитрификации развиваются в чистом пару, где в течение лета в черноземах, темно-серых лесных и лугово-черноземных почвах накапливается 120-170 кг/га нитратного азота. Такого количества азота при наличии других элементов питания достаточно для получения урожая зерновых культур в 30-40 ц/га. Роль пара как накопителя нитратов снижается на почвах с небольшим содержанием органического вещества каштановых, светло-серых лесных и дерново-подзолистых почвах. Однако и в этих почвах в паровом поле содержится больше нитратного азота, чем в других полях севооборота.
Значительное накопление нитратного азота после августовской вспашки пласта многолетних трав, после хорошо обрабатываемых пропашных культур, после рано убираемых многолетних трав. По этим предшественникам на высокогумусных почвах обычно нет необходимости в дополнительном внесении азотных удобрений.
В черноземах активность накопления этой формы азота обычно в 2-4 раза выше, чем в дерново-подзолистых и серых лесных почвах. В дерново-подзолистых почвах количество азота возрастает от весны к июлю августу и практически остается неизменным до осени. В черноземных почвах в период июня июля темпы накопления нитратного азота вследствие засушливых условий замедлены: резкий подъем нитратообразования в них наблюдается в увлажненную вторую половину лета (июль-август). Под сельскохозяйственными культурами содержание нитратного азота весьма динамично, поскольку растения используют его в качестве азотной пищи. Количество нитратного азота несколько возрастает после уборки урожая.
Режим нитратного азота в значительной степени определяется способами основной обработки почвы. Сокращение глубины и числа обработок приводит к снижению накопления нитратов.
Основные биохимические этапы миграции и трансформации нитратного азота следующие:
1. Биологическое поглощение. Нитратный азот находится в почвенном растворе в качестве аниона, легко поглощается и усваивается в основном биологическим путем.
2. Денитрификация. В анаэробных условиях бактерии рода Pseudomonas, Denitrifican, Fluorensens, ответственные за процесс денитрификации, восстанавливая нитратный азот до закисных, летучих форм, молекулярного азота на каждом из этапов добывают кислород для дыхания. Этот процесс наиболее интенсивно происходит в условиях парового поля в виду наличия в почве свободных нитратов, анаэробиозиса, щелочной реакции и избытка органического вещества. Активные расы денитрификаторов являются термофильными бактериями, оптимальная температура для них выше 25 0 С.
3. Вымывание вынос нитратного азота в почвенном растворе из корнеобитаемого слоя почвенного профиля. В случае смыкания инфильтрационных вод с грунтовыми этот азот теряется безвозвратно. При глубоком залегании грунтовых вод в последующем возможен подъем нитратного азота восходящим током влаги и по градиенту концентрации.
3. Некоторые особенности питания растений нитратным и аммиачным азотом.
Эффективность азотного питания обусловливается формами азотных соединений и условиями их применения. В нейтральной среде обычно лучше проявляется действие аммиачного азота, чем нитратного. Калий и натрий способствуют большему поглощению нитратов, кальций и магний обеспечивают лучшее усвоение аммиака растениями. Для синтеза органических веществ растения используют аммиачный азот быстрее, чем азот нитратов. Преимущество аммиачного питания по сравнению с нитратным в том, что аммиачный азот стоит ближе к продуктам синтеза азотсодержащих веществ в растениях. Для синтеза аминокислот требуется восстановленная форма азота. Нитраты, прежде чем стать непосредственными продуктами синтеза аминокислот и белков, должны быть восстановлены внутри растений до аммиачного азота. При наличии достаточного количества углеводов в растениях нитраты восстанавливаются уже в корнях. Процесс ферментативного восстановления нитратов в растениях идет благодаря окислению углеводов. Нитраты восстанавливаются до аммиака с помощью ферментов, которые представляют собой металлофлавопротеиды. Для них необходимы такие элементы, как молибден, медь, железо, марганец, особенно важен молибден.
Аммиачный азот, поступивший в растения или образовавшийся в них в результате восстановления нитратов и нитритов, не накапливается в них. Накопление аммиачного азота может вредить растениям только в молодом возрасте.
В жизни растения большую роль играет процесс образования аминокислот прямым аминированием кетокислот. Аминокислоты способны передавать свои аминные группы кетокислотам; в этом случае протекает реакция переаминирования, т. е. аминогруппа аминокислот переходит в кетокислоту и в результате образуются аминокислоты. Переаминирование особенно важно для синтеза белков а также для процесса дезаминирования аминокислот, когда идет образование кетокислот и аммиака.
Полученные таким образом кетокислоты в растениях участвуют в образовании углеводов, жиров и других веществ. Аммиак принимает участие в образовании аминокислот в результате прямого аминирования кетокислот, которые получаются из углеводов. Кроме того, из аммиака образуются амиды аминодикарбоновых кислот аспарагин и глютамин. В результате этого процесса происходит обезвреживание аммиака при обильном аммиачном питании и при недостатке в растениях углеводов, а также при его накоплении в процессе дезаминирования аминокислот.
В отдельных растениях (щавель, осока, хвощ и др.), в которых накапливается значительное количество органических кислот, аммиак может обезвреживаться благодаря образованию аммонийных солей. Например, взаимодействие аммиака со щавелевой кислотой дает щавелевокислый аммоний. Кроме того, возможно обезвреживание аммиака при образовании в растительных тканях мочевины.
Наряду с синтезом белков в растениях идут процессы их распада через аминокислоты до аммиака. Таким образом, с одной стороны, аммиак, поглощенный растением или образовавшийся в результате восстановления нитратов, служит первичным исходным материалом для синтеза белков, с другой стороны, конечным продуктом распада белков.
Процессы азотного обмена веществ происходят в течение всего роста и развития растений. Характер их зависит от вида и возраста растений, условий среды, в частности условий питания, и других факторов. В молодых растениях синтез белков значительно преобладает над их распадом.
Исследования, осуществленные с помощью изотопа 15 N , показали, что в молодых растениях азот белка обновлялся полностью всего за три дня, а в старых листьях обновлялось лишь около 12% белкового азота за 12 дней. Отношение растений к аммиачному и нитратному питанию зависит от их обеспеченности углеводами. Растения, которые содержат малый запас углеводов в семенах, например, свекла, значительно хуже переносят избыток аммиака, чем нитратов. Картофель, в клубнях которого большой запас углеводов, способен переносить высокие дозы аммиака. Таким образом, для нормального роста и развития растений требуются определенные условия их питания как нитратным, так и аммиачным азотом.
В растения азот поступает неравномерно. В ранние фазы развития растения характеризуются высоким содержанием азота.
В этот период они особенно требовательны к условиям минерального питания. Биологические особенности отдельных растений определяет характер поступления в них питательных элементов. Величина усвоения азота растениями зависит от формы удобрений, температуры, влажности почвы, показателя рН и других условий, но, как правило, не превышает 30-50% (по средним показателям полевых опытов с I5 N).
С понижением температуры наблюдается более сильное снижение поглощения растениями азота окисленных форм удобрений по сравнению с восстановленными. При этом в корнях растений накапливаются нитраты вследствие ингибирования процессов их восстановления и передвижения в надземные органы. В условиях пониженной температуры при аммиачном питании процессы синтеза аминокислот протекают более интенсивно, чем при нитратном, когда больше накапливается углеводов.
На поглощение корнями аммиачных или нитратных ионов влияет также аэрация и величина рН окружающего раствора. С ростом исходного рН поглощение корнями нитратов уменьшается, а аммония возрастает, при любом рН корни больше поглощают NH 4 + , чем NО 3 - . Аэрирование усиливает поглощение ионов аммония и не влияет на поглощение нитратов.
Величина усвоения растениями азота удобрений при низком содержании подвижных форм фосфора и калия меньше на 10 15%, чем при внесении фосфорных и калийных удобрений.
Использование азота удобрений растениями зависит от сроков их применения. Так, на дерново-подзолистой почве при внесении азотных удобрений в фазы выхода в трубку и колошения пшеница использует 45 50% меченого азота, а в фазу молочной спелости не более 10%.
Поглощенный неорганический азот в определенной последовательности включается в синтез азоторганических соединений сначала образуются более простые, затем, более сложные соединения (конституционные и запасные белки). При фосфорном голодании скорость включения азота в азотистые фракции заметно снижается, при этом тормозится его поглощение и передвижение в надземные органы.
В условиях недостатка кислорода нитратный азот используется только в процессе синтеза белка. В аэробных условиях преимущество имеет аммиачный азот, что особенно важно при выборе ассортимента азотных удобрений для почв, обеспеченных в различной степени кислородом.
При внесении в почву азотных удобрений растения лучше и больше усваивают азот самой почвы. Это обусловлено мобилизацией азота органического вещества почвы, в результате чего он становится более доступным растениям. На хорошо окультуренных дерново-подзолистых почвах больше поступает в растения азота из самой почвы, чем на слабоокультуренных, что важно при разработке прогноза эффективности доз удобрений для почв различного уровня плодородия.
Наряду с использованием растениями азота удобрений часть его закрепляется в почве в органической форме, а также теряется в виде газообразных соединений. Такие процессы происходят в основном впервые 20 30 дней, когда азот еще не полностью использован растениями и подвергается интенсивному воздействию гетеротрофных микроорганизмов, а также нитрифицирующих и денитрифицирующих бактерий. Как правило, закрепление азота в органической форме из нитратных удобрений меньше, чем из аммиачных и мочевины. Потери же, наоборот, возрастают при использовании нитратных удобрений. На кислых почвах, в которых накапливаются нитраты, потери внесенного азота могут достигать 55%. Возможны потери азота при фотоокислении органического вещества, а также благодаря биологической денитрификации. В результате процесса окисления нитрификации аммиака потери азота из почвы наблюдаются даже в нейтральной и слабощелочной среде. Под влиянием негумифицированного органического вещества клетчатки и других углеводов потери азота удобрений из почвы сокращаются в 2-3 раза. При отношении углерода органического вещества к азоту удобрений, равном 30, потери азота удобрений с избытком компенсируются его фиксацией. Один из путей снижения потерь азота применение ингибиторов, избирательно действующих на нитрифицирующие микроорганизмы. Потери азота удобрений снижаются в 1,5-2 раза при внесении их вместе с ингибиторами, причем в 2 раза возрастает закрепление азота в органическом веществе почвы.
Полноценное азотное питание при обеспеченности другими элементами, особенно фосфором и калием, способствует улучшению роста и развития растений. В то же время усиленное азотное питание при недостатке фосфатного и калийного очень часто приводит к неравномерности созревания культур, их полеганию, снижению сопротивляемости к грибным болезням и неблагоприятным климатическим условиям. В таких случаях необходимо обеспечить растения фосфором, калием, а также отдельными микроэлементами. Рациональное применение азотных удобрений на фоне фосфорно-калийных и высокой агротехники обеспечивает оптимальное развитие сельскохозяйственных растений и в результате получение высоких урожаев хорошего качества.
4.Баланс азота.
Пути накопления азота в почве следующие:
а) неисчерпаемым источником азота является атмосфера (среди прочих газов атмосферы на молекулярный азот приходится 78%. Однако молекулярный азот, будучи инертным газом, не может непосредственно усваиваться растениями.
б) фиксация молекулярного азота и пополнение запасов его в почве осуществляется двумя путями: под влиянием грозовых разрядов и с помощью определенных микроорганизмов. Под действие электрических и фотохимических реакций при грозах образуются аммиак и окислы азота, которые поступают в почву с атмосферными осадками. По данным А.В.Петербургского (1979), в осадках всегда больше аммонийного, чем нитратного азота, и общий приход его достигает в среднем около 4кг/га*год.
в) Гораздо большее значение в обогащении почв азотом имеет биологическая фиксация атмосферного азота свободноживущими микроорганизмами, сине-зелеными водорослями и клубеньковыми бактериями. Потенциальные возможности симбиотических и несимбиотических свободноживущих азотфиксаторов неравноценны. Свободноживущие азотфиксирующие микроорганизмы способны при благоприятных условиях ассимилировать 10-15 кг/га*год связанного азота. Клубеньковые бактерии поглощают значительно больше азота из атмосферы. По данным Д.Н.Прянишникова (1945), ежегодно на 1 га люцерна накапливает 300(до 500-600), клевер 150-160 (до 250-300), люпин до 150, соя до 100, вика, горох- 50-60 кг азота. Количество фиксированного азота зависит от вида бобового растения Ph почвенного раствора, величины урожая. Наиболее активно азотфиксация осуществляется в фазу цветения бобовых культур.
г) В связи с развитием химизации земледелия существенная роль в обогащении почв азотом принадлежит так называемому «техническому азоту».
Потери азота (статья расходования элемента)
а) Аммонийный и нитратный азот легко вовлекается в процессы биологического поглощения, поэтому значительное их количество выносится с урожаем полевых растений.
б) Газообразные потери аммонийного азота, которые происходят из хорошо аэрируемой почвы при ее периодическом высыхании и увлажнении.
в) вынос аммонийного азота в составе почвенных коллоидов при эрозионных процессах, количество которого определяется массой смытой почвы и содержанием аммония в ней.
г) вымывание аммонийного и нитратного азота происходит в составе почвенного раствора, а также и аммонийного азота в поглощенном состоянии в коллоидах – мигрантах.
д) денитрификация процесс разрушения нитратного азота и восстановление его до молекулярной формы. При недостатке кислорода, в условиях избытка свежего органического вещества бактерии рода Denitrificator с помощью ферментов нитратредуктазы осуществляют восстановление нитратного азота до молекулярного.
Этот процесс возникает и особенно интенсивно развивается в условиях, когда в почве отсутствует воздух, почва имеет щелочную реакцию и в избытке неразложившееся органическое вещество богатое клетчаткой, глюкозой и другими углеводами. Денитрифицирующие бактерии быстро окисляют органическое вещество, используя для этой цели кислород нитратов. Процесс восстановления нитратов носит эндотермический характер, т.е реакция протекает с затратой энергии.
е) иммобилизация азота вторичные процессы синтеза, когда минеральные соединения азота вновь переходят в органические, не усвояемые для растений. Эти процессы носят биологический характер. Микроорганизмы строят белок своих тел, используя углеводы и азот. Различные бактерии, актиномицеты, плесневые грибы разлагают клетчатку, пентозаны и другие вещества растительных и животных остатков. В качестве азотной пищи им необходимы в первую очередь легкорастворимые соединения азота почвы, которые они переводят в белок плазмы клеток. При отмирании бактерий азот снова переходит в форму минеральных соединений аммиака и нитратов.
ж) необменное поглощение аммиачного азота минералами с трехслойным строением кристаллической решетки.
Фосфор почвы. Содержание и формы фосфора. Доступность почвенных фосфатов растениям. Пути накопления и потерь фосфора
История «путешествий» фосфора на Земле, или, как говорят ученые-геохимики, его миграция, очень интересна и поучительна. Атомы фосфора, как и всех других элементов, постоянно участвуют в великом природном круговороте веществ.
Фосфор относительно редкий элемент. По данным академика А.Е.Ферсмана, его весовой кларк (процентное содержание элемента в земле) равен всего 0,12%. В таблице распространенности химических элементов в земной коре он стоит на 13-м месте вслед за углеродом и хлором, перед серой. К тому же фосфор элемент, редко накапливающийся в больших количествах, и потому его относят к числу рассеянных.
В свободном виде в природе по причине своей очень сильной окисляемости он не встречается, но входит в состав многих минералов (их насчитывается до 120) и множества органических веществ. Большинство минералов, содержащих фосфор, являются редкими. Наиболее важные минералы (природные фосфаты) апатит, вивианит, а также осадочная горная порода фосфорит (состоит из мелкокристаллического или аморфного фосфата кальция с примесью некоторых других веществ).
Несмотря на свою малую распространенность и разбросанность, фосфор, однако, имеет исключительно важное значение в жизни растительных и животных организмов. Он входит в состав большинства растительных и животных белков и протоплазмы. Фосфор биогенный элемент. Академик Ферсман называл фосфор элементом жизни и мысли.
Источником всех фосфорных соединений в природе следует признать апатит фосфат кальция, содержащий переменное количество фтора и хлора. В зависимости от преобладания в апатите фтора или хлора образуются минералы фторапатит Са 5 F(РO 4) 4 или хлорапатит Са 5 Сl(PO 4) 3 . Они содержат от 5 до 36% P 2 O 5 .
Рисунок. Мировое месторождение апатитов в Хибинах
В изверженных породах обычно всегда есть мелкие кристаллики апатита. Главнейшие его запасы находятся в зоне магмы, но он встречается и в тех местах, где изверженные породы образуют контакт с осадочными. Значительные запасы апатитов имеются в Норвегии и Бразилии. Подлинно мировое месторождение апатитов находится у нас, на Кольском полуострове, в Хибинах, где оно было открыто в 1925 г.
Под влиянием жизнедеятельности микроорганизмов, почвенных кислот, а также кислот, выделяемых корнями растений, апатиты постепенно подвергаются выветриванию и вовлекаются в биохимический круговорот, который в отличие от круговорота азота, углерода, кислорода и серы ограничивается лишь био-, гидро- и литосферой и не захватывает атмосферы.
Растениями фосфор поглощается только из растворенных фосфатов в виде анионов фосфорной кислоты. Поэтому питание фосфором растений возможно лишь при наличии в почвенном растворе солей фосфорной кислоты, например Са(Н 2 РО 4) 2 , СаНРО 4 , К 2 НРО 4 и др. Скапливается он главным образом в продуктовых частях семенах, плодах. Наиболее богаты фосфором бобовые растения, а бедны им овощи. Из растений фосфор вместе с пищей попадает в организм животных и человека.
В теле человека имеется свыше 1,5 кг фосфора (1,4 кг в костях, 130 г в мышечных и 12 г в нервных тканях). Ежесуточная потребность взрослого человека в фосфоре от 1 до 1,2 г. Дети больше нуждаются в фосфоре, чем взрослые. По подсчетам ученых, с каждым куском хлеба весом 100 г человек поглощает до 1022 атомов фосфора, т.е. такое астрономическое число, которое не только невозможно представить, но даже и выразить обычными словами. Больше всего его содержится в костях (свыше 5%). Твердость скелету придает кальциевая соль фосфорной кислоты. Очень много фосфора в зубах (в дентине 13%, а в зубной эмали 17%). При недостатке фосфора у животных появляется заболевание костей.
При разложении богатых фосфором органических соединений могут образоваться газообразные и жидкие вещества. В частности, аналогично аммиаку может образоваться очень ядовитый бесцветный с чесночным запахом газ фосфористый водород, или фосфин, РН3. Этот газ можно получить в лаборатории при кипячении белого фосфора с едким кали или при действии соляной кислотой на фосфид кальция: Са 3 Р 2 + 6НСl = 3СаСl 2 + 2РН 3 .
Одновременно с фосфином при этой реакции часто образуется в небольшом количестве жидкий продукт соединения фосфора с водородом дифосфин Р 2 Н 4 , пары которого сами собой воспламеняются при обычной температуре и поджигают газообразный фосфин.
Подобного рода процессы происходят и в природе, являясь причиной появления так называемых «блуждающих огней» на кладбищах. Вспышки фосфина днем, конечно, не бывают видны, но ночью они вызывают суеверный страх у многих людей, которые незнакомы с научным объяснением этого явления. Описание «блуждающих огней» дано в «Вечерах на хуторе близ Диканьки» Н.В.Гоголем в рассказе «Заколдованное место». Жидкий дифосфин, выделяясь на болотах вместе с метаном, поджигает последний, и тогда возникает новое «чудо» блуждающие болотные огни. Роль подобных процессов в природе относительно незначительна. Наоборот, образование различного рода фосфатов происходит в очень больших масштабах.
Существует несколько объяснений, как могли образоваться громадные накопления фосфатов органического происхождения, поскольку причины, вызывающие этот процесс, различны.
Богатый фосфором птичий помет, известный под названием гуано, в условиях сухого климата скапливается иногда в огромных количествах. Так, например, на островах Тихого океана, в Чили и Перу имеются огромные толщи гуано (до 100 м). Гуано одно из самых эффективных удобрений. Оно содержит до 9% азота и 3% фосфорной кислоты.
Большие скопления помета имеются и в пещерах, где обитают летучие мыши. В процессе различных химических превращений эти вещества постепенно образуют различные минералы (алюмофосфаты, монофосфаты и др.). Образование залежей подобных соединений может произойти и в результате различных геологических катастроф, приводящих к массовой гибели животного мира.
Значительным признанием пользуется так называемая биолитная гипотеза происхождения фосфоритов. Согласно ей их залежи могли образоваться в результате массовой гибели морской фауны при встрече теплого морского течения с холодным: быстрая смена температуры оказывает одинаково гибельное влияние на животных, населяющих воды того и другого течения и не приспособившихся к быстрой смене условий. Гибель животного мира может происходить и при встрече течений с различной степенью содержания солей в их водах, например в дельтах больших рек, впадающих в моря и океаны.
В 1934 г. русский ученый А.В.Казаков опубликовал химическую гипотезу происхождения фосфоритов в морских водах. По этой гипотезе фосфаты, растворенные в морской воде, начинают осаждаться, когда из глубин моря они выносятся на его поверхность. Происходит это вследствие уменьшения кислотности воды (в связи с удалением части углекислоты); растворимость фосфатов в этой среде уменьшается, и тогда избыток их выпадает на дно. Так и образовались мощные залежи фосфоритов, оказывающиеся затем на суше вследствие геологических катастроф или постепенного поднятия морского дна.
Фосфоритовые залежи есть во многих странах. Наиболее известны месторождения в Северной Африке (Египет, Тунис, Алжир, Марокко), в США (Флорида). В России месторождения фосфоритов распространены на Урале, в Поволжье, Московской, Кировской, Смоленской, Брянской, Ленинградской и других областях.
В процесс круговорота фосфора, как и в природный круговорот других элементов (кислорода, азота, серы, калия, кальция, алюминия, железа и др.), энергично вмешивается человек. Фосфор нужен человеку для многих целей: большое количество его поглощает спичечная отрасль промышленности. Лучшие сорта нержавеющей стали получаются благодаря процессу фосфатирования – покрытия тонким слоем фосфатов, стойких против атмосферной коррозии. Аналогичной обработке часто подвергаются изделия из цинка, алюминия и их сплавов. Соединения фосфора идут на изготовление многих лекарственных веществ.
Главный же потребитель фосфатов сельское хозяйство. Со времени химика Ю.Либиха земледельцы, поняв значение фосфора для повышения урожая культурных растений, начали отыскивать природные фосфаты (апатиты, фосфориты), превращать их механическим или чаще всего химическим путем в удобрения и вносить в почву.
Важно заметить, что в 100 кг пшеницы находится около 1 кг фосфора (в виде Р 2 О 5). Столько же фосфора содержится в 200 кг сена, 300 кг соломы, 1500 кг зеленых кормов. Можно себе представить, какие громадные количества фосфора уносятся с наших полей вместе с урожаем. Часть его, конечно, возвращается в почву, но фосфор, например, содержащийся в продуктовых частях растений, идущих на промышленную переработку, пропадает. Не обладая бесконечными запасами фосфора, почва вследствие этого процесса постепенно истощается, что приводит к сильному снижению урожая и необходимости восполнения потери фосфора. Культурные растения в большинстве случаев очень благоприятно отзываются на внесение в почву фосфорных удобрений в легкоусвояемой форме.
Рисунок. Круговорот фосфора в природе
Фосфорное удобрение получается также в качестве побочного продукта при переработке богатого фосфором чугуна в сталь при томасовском процессе. Если «грушу», в которой получается сталь по методу Г.Бессемера, выстлать внутри известковой футеровкой, то известь поглотит фосфор из расплавленного чугуна. В этом и состоит сущность предложенного англичанином С.Дж.Томасом процесса, при котором сразу достигаются две цели: получение доброкачественной стали и ценного удобрения. Последнее достигается путем размалывания поглотившей фосфор известковой футеровки. Получаемый таким путем сухой темно-серый порошок, называемый томасшлаком, содержит от 11 до 24% Р 2 О 5 и является высокоэффективным удобрением, особенно на кислых почвах.
Главнейшие процессы, характеризующие круговорот фосфора в природе, изображены на рисунке. Объяснением этого рисунка могут служить следующие слова знаменитого русского геолога и минералога, профессора Я.В.Самойлова, которому принадлежит большая заслуга в деле изучения фосфоритов: «Фосфор наших фосфоритовых месторождений биохимического происхождения. Из апатита минерала, в котором первоначально заключен почти целиком весь фосфор литосферы, элемент этот переходит в тело растений, из растений в тело животных, которые являются истинными концентраторами фосфора. Пройдя через ряд животных тел, фосфор, наконец, выпадает из биохимического цикла и вновь возвращается в мир минеральный. При определенных физико-географических условиях в море происходят массовая гибель животных организмов и скопление их тел на дне морском, а скопления эти приводят к образованию фосфоритовых месторождений в осадочных отложениях. Наши фосфориты биолиты, и если бы можно было шаг за шагом повернуть весь ход испытанных нашими фосфоритами перемещений в обратную сторону, то образцы, заполняющие наши музеи, зашевелились бы... »
Таким образом, основные запасы фосфора сосредоточены в горных породах земной коры, в донных осадках морей и океанов, а также в гумусовом горизонте почвы. Главными источниками поступления фосфора в почву являются материнские породы (60% запасов фосфора находится в минеральной части твердой фазы почвы), органические остатки растительного и животного происхождения, органические и минеральные удобрения. В почвах найдено более 200 различных минеральных соединений фосфора. Преобладающими фосфорсодержащими соединениями в земной коре являются разновидности минерала апатита, главным образом, фторапатита.
Глобальный биогеохимический круговорот большинства биогенных макроэлементов предполагает наличие у них газовых форм. И только фосфор, не имея газовых форм, необратимо вымывается в океан. Возврат элемента в геологическом масштабе осуществляется, когда дно моря становится сушей: основные месторождения фосфатов бывшие донные отложения органического происхождения.
6.Доступность почвенных фосфатов растениям (условия, определяющие их растворимость).
В результате биологического круговорота фосфора в почве накапливаются органические фосфаты , доля которых может достигать до 80% от общего содержания фосфора. Прямым источником органического фосфора являются такие устойчивые соединения, как нуклеопротеиды, нуклеиновые кислоты, фосфатиды, фитин и их производные. Выделяют две группы органических фосфатов в почве: неспецифические соединения индивидуальной природы, образующиеся в результате биологического синтеза и фосфогумусовые специфические соединения. Содержание фосфора в составе специфических гумусовых веществ составляет (в %): в серых лесных почвах 1,78- 2,46; в черноземе обыкновенном -0,9-1,27; в черноземе выщелоченном -1,1-1,43; в темно-каштановой -0,97-1,3. В почве одновременно протекают разнонаправленные процессы. Происходят иммобилизация органическим веществом фосфора почвенного раствора и минерализация органических веществ, которая сопровождается поступлением фосфора в почвенный раствор. Фосфор плазмы микроорганизмов входит в состав белковых тел микроорганизмов. Эта форма фосфора не выполняет существенной роли в питании растений до тех пор, пока из-за неблагоприятных условий обитания микроорганизмы не погибнут. Поскольку, в благоприятных условиях фосфор передается дочерним поколениям при делении клетки материнской особи.
Минеральные формы фосфора находятся преимущественно в виде соединений ортофосфорной кислоты с ионами кальция, магния, железа и алюминия. Соли фосфорной кислоты наиболее доступная для растений и распространенная форма фосфора в почве, составляет до 5% от валового его содержания. Образуется в результате минерализации органических соединений с помощью фермента фосфатазы или при выветривании минералов. Доступность растениям фосфатов почвы определяется степенью замещенности водородных ионов ортофосфорной кислоты: Ca(H 2 PO 4) 2 однозамещенный фосфат кальция, растворим в воде; CaHPO 4 двузамещенный фосфат кальция, растворим в слабокислой среде; Ca 3 (PO 4) 2 трехзамещенный фосфат кальция, слабо растворим в кислой среде. Значительная их доля адсорбируется на «+» заряженной частью почвенного поглощающего комплекса (базоидами).
Уровень фосфорного питания растений зависит от растворимости минеральных форм фосфора. Фосфаты кальция становятся нерастворимыми в щелочных условиях, а фосфаты железа и алюминия в кислых. Таким образом, химическое осаждение фосфатов из растворов и сорбция их на поверхности почвенных частиц определяется характером реакции почвенного раствора, обуславливая преобладание одного из трех ионов фосфора.
В интервале кислых и нейтральных почв преобладает монофосфат одновалентный ортофосфат H 2 PO 4 , в щелочной среде при pH выше 7,2 доминирует HPO 4 . Ион PO 4 появляется при pH выше 10. Так, растворимость фосфатов полуторных окислов возрастает по мере повышения pH раствора, и, наоборот, в кислой среде они приобретают кристаллическое строение со значительной потерей растворимости. При pH=5 фосфор преимущественно связывается с кальцием, растворимость фосфатов кальция возрастает по мере подкисления среды. Осаждение фосфатов железа происходит при рН ниже 3,5; фосфатов алюминия - ниже 5; а кальций фосфатов - при рН выше 7,5 (Томпсон, Троу, 1982). Возможность осаждения и растворения этих соединений при различных значениях реакции среды может быть представлена в виде схемы представленной выше. Наиболее легко абсорбируется растениями монофосфат. Таким образом, вследствие высокой активности элементарного фосфора и его окислов он образует мало- и труднорастворимые соединения в воде. Т.е. проявляется химическое осаждение фосфатов из растворов и сорбция их на поверхности почвенных частиц. Это явление известно как химическое поглощение фосфора (ретроградация) и определяет эффективность фосфорных удобрений.
Исследованиями установлено, что кроме перечисленных факторов увлажнение-высушивание почвы приводит к «распаковке» глинистых минералов с трехслойным строением кристаллической решетки и высвобождению фосфора. Быстрое смачивание почвы способствует разрушению почвенного агрегата, обнажению внутренних его поверхностей, а, следовательно, и переходу в почвенный раствор ранее скрытых соединений фосфора. Кроме того, степень обеспеченности растений доступными почвенными фосфатами зависит от уровня потребления фосфора возделываемой культурой и связано с ее биологическими особенностями. По данным Д.Н.Прянишникова, некоторые растения (гречиха, горчица, эспарцет, донник, горох) способны усваивать фосфор из трехзамещенных фосфатов. На усвоении фосфатов большое влияние оказывают аммиачное и аммиачно-нитратное удобрения. Поскольку, аммиачные формы азотных удобрений обладают физиологической кислотностью, последняя может оказать растворяющее воздействие на фосфорит.
Исходя из особенностей взаимодействия различных почв с фосфором удобрений, характера превращения фосфора в почвах приемы рационализации фосфатного режима почвы представляются следующими:
- Уменьшение контакта водорастворимых фосфатов с почвой (грануляция, капсулирование, локальное и припосевное внесение).
- Активизация слаборастворимых фосфорных удобрений при взаимодействии с кислым субстратом (фосфоритование кислых почв, компостирование фосфоритной муки с навозом).
- Активизация фосфора самой почвы путем известкования, фаворизации деятельности микроорганизмов, разрушающих органофосфаты, фосфаты железа, кальция и алюминия.
7. Баланс фосфора.
В органической форме фосфор входит в состав сложных белков (нуклеопротеидов), нуклеиновых кислот, фосфатидов, фитина, фосфорных эфиров, Сахаров, В-ферментов и других биологически активных веществ. Значительное количество фосфора находится в растениях в минеральной форме и используется в различных реакциях фосфорилирования (превращение углеводов с участием фосфорной кислоты).
Соединения фосфора с аделиновой кислотой (аденизиндифосфаты и аденизинтрифосфаты) занимают ведущее место в энергетическом обмене в клетке. Они богаты макроэргическими связями, в которых аккумулируется энергия, освобождающаяся при дыхании растений и используемая в разнообразных процессах синтеза.
Основным источником фосфатного питания растений в природных условиях служат соли ортофосфорной кислоты. Пирофосфаты и метафосфаты также могут быть использованы сельскохозяйственными культурами.
Соли одновалентных катионов ортофосфорной кислоты хорошо растворимы в воде и легко усваиваются растениями так же, как и соли двухвалентных катионов ортофосфорной кислоты, если они замещают в кислоте один водород (главным источником таких соединений служит суперфосфат, содержащий в своей основе мококальцийфосфат). Соли двухвалентных катионов (например, дикальцийфосфат) нерастворимы в воде. Однако они хорошо растворяются в слабых кислотах, в том числе и органических, которые присутствуют в почве.
Трехзамещенные ортофосфаты двухвалентных катионов (например, трехкальциевый фосфат) практически нерастворимы в воде, очень слабо растворимы в слабых кислотах и плохо усваиваются растениями. Но такие культуры, как люпин, гречиха, горчица, эспарцет, горох и конопля, способны достаточно хорошо усваивать трехкальциевые фосфаты и тонкоразмолотые фосфориты.
Очень слабо используется растениями фосфор средних и особенно основных солей трехвалентных катионов ортофосфорной кислоты. Органические фосфорные соединения при воздействии ферментов микрофлоры переходят в минеральные фосфаты, которые и усваиваются растениями. Растения поглощают фосфаты более интенсивно в первый период роста, чем в последующие. Недостаток фосфорного питания в ранний период роста растений очень сильно сказывается на дальнейшем их развитии. При этом фосфорное голодание в начале развития растения невозможно полностью преодолеть последующим внесением фосфора. Более того, обильное фосфорное питание в дальнейшем отрицательно сказывается на развитии сельскохозяйственных культур.
Исследования с применением радиоизотопов фосфора позволили установить большую скорость передвижения фосфатов из почвы в растения и внутри них. Фосфор, поступающий в растение, очень неравномерно распределяется между его органами и тканями. Растущие клетки получают фосфора больше, чем клетки, деление которых прекратилось. В фазу созревания репродуктивных органов к ним очень энергично передвигаются фосфаты из вегетативных частей. Основная часть фосфора сосредоточивается в товарной части урожая. Отсюда вытекает необходимость заботиться о достаточном обеспечении фосфорным питанием сельскохозяйственных культур. При нормальном питании злаковых культур фосфатной пищей ускоряется их развитие и созревание, повышается сопротивляемость к полеганию, а также улучшается качество продукции.
Калий почвы. Содержание и формы калия. Доступность почвенного калия растениям. Баланс калия в земледелии
Калий содержится в почвах главным образом в алюмосиликатах. Валовое содержание калия в почвах выше, чем азота и фосфора. Оно определяется, прежде всего, минералогическим и гранулометрическим составом почвы. Объясняется это тем, что большая часть почвенного калия входит в состав полевых шпатов, слюд и различных глинистых минералов (иллит, монтмориллонит, вермикулит). Полевые шпаты (ортоклаз, роговая обманка, микроклин) распространены весьма широко на них приходится 60% минералогического состава поверхностного слоя земной коры. В их составе 10-12% занимает оксид калия. Большое распространение имеют калийные слюды - мусковит, биотит, флогопит. Мусковит содержит в среднем 10%, а биотит 8% оксида калия. В результате выветривания и биохимического разрушения полевых шпатов и слюд образуются гидрослюды (вторичные минералы). Они входят в состав преимущественно дисперсных фракций почвы. Поэтому, содержание калия в почвах зависит от их гранулометрического состава. Почвы тяжелого гранулометрического состава могут фиксировать значительно больше калия, чем легкие. Помимо минералогического и гранулометрического составов на поглотительную способность почвы в отношении калия значительное влияние оказывают ее влажность, содержание гумуса, реакция среды, биологическая активность, а также дозы и формы минеральных удобрений. В почве калия много в составе живого и мертвого органического вещества, поэтому на содержание калия в почве оказывает влияние степень гумусированности. Меньше всего калия содержится в торфяниках и песчаных почвах, в легких подзолистых и дерново-подзолистых почвах. Максимальные запасы элемента сконцентрированы в черноземах, каштановых и сероземных почвах.
В пахотном слое дерново-подзолистых, песчаных и супесчаных почв находится 0,6-1,5% валового калия (К 2 О), в глинистых- 1,5-2,5%. В серых лесных и черноземных почвах количество валового калия достигает 1-3%, в каштановых и бурых почвах-1-2%.
В почвах различают три формы соединений калия водорастворимый, обменный и необменный, входящий в состав силикатов.
Растения могут усваивать не только водорастворимый и обменный калий, но частично и необменный (на тяжелых почвах в большей степени, чем на легких). Запасы подвижного калия пополняются в результате выветривания минералов. С другой стороны, обменный калий в почве может переходить в необменные формы.
Агрохимическое обследование почв России показало, что они довольно хорошо обеспечены подвижным калием. Около 67% пахотных почв характеризуется повышенным, высоким и очень высоким его содержанием и лишь 10,8% очень низким и низким. Почвы отдельных природно-экономических районов значительно различаются по количеству подвижного калия. Однако в целом почвы всех районов более обеспечены калием, чем фосфором. Особенно бедны обменным калием легкие подзолистые и торфяные почвы.
В лесной подзолистой зоне преобладают пахотные почвы с низким и средним содержанием обменного калия и только 3% с очень низким. Свыше 30% почв имеет повышенное, высокое и очень высокое его содержание. Наименее обеспечены обменным калием почвы Центрального района Нечерноземной зоны, где почти 32% земель с низким и 5% с очень низким его содержанием.
Наибольшее количество обменного калия находится в пахотных почвах Уральского района, здесь 60% земель имеют повышенное, высокое и очень высокое его содержание. Правда, этот район не полностью входит в зону подзолистых почв.
Закономерности размещения почв с различным содержанием калия еще недостаточно ясны. По-видимому, здесь большую роль играют провинциальные литологические особенности почвообразующих пород. Определенное значение имеют и различия в механическом составе почв. Влияние окультуренности почв на содержание калия сказывается слабее, чем на содержание фосфора. Иногда более окультуренные почвы с повышенным количеством фосфора содержат даже меньше калия, чем менее окультуренные.
Для правильного суждения об обеспеченности почв подвижным калием и его доступности растениям необходимо знать не только его содержание, но и степень подвижности. При одном и том же количестве обменного калия степень его подвижности в легких почвах выше, чем в тяжелых. Источником накопления обменного калия по мере его использования служит необменный калий. В легких дерново-подзолистых почвах значительно меньше необменного калия по сравнению с тяжелыми. Наибольшим его количеством обладают пойменные почвы.
Черноземные почвы Центрально-Черноземной зоны лучше обеспечены подвижным калием, чем почвы подзолистой зоны. Особенно много его в черноземах Западно-Сибирского района (56% земель с очень высоким содержанием). Количество обменного калия здесь увеличивается от лесостепи к сухим степям, достигая наибольшей величины в южных черноземах. Почти во всех каштановых почвах, за исключением супесчаных и песчаных разновидностей, отмечено значительное количество подвижного калия. Особенно богаты им почвы Прикаспийской низменности. Достаточно обеспечены подвижным калием почвы Восточной Сибири и Дальнего Востока, где размещено свыше 60% пахотных земель с повышенным, высоким и очень высоким его содержанием.
9. Формы и доступность почвенного калия растениям
По степени доступности растениям почвенный калий классифицируется следующим образом (Панников, Минеев, 1977). Не все формы калия в почвах доступны растениям. Общепринятым считается, что все формы калия находятся в динамическом равновесии. Принято выделять следующие формы: водорастворимый, обменный, фиксированный, калий нерастворимых силикатов, калий органической части почвы.
Валовое содержание калия в почвах выше, чем азота и фосфора. Объясняется это тем, что калий входит в состав большинства минералов, слагающих почвообразующую породу. Однако валовое содержание элемента не характеризует то его количество, которое может быть усвоено растениями. Эта форма элемента определяется как калий, входящий в состав кристаллической решетки почвенных минералов, она практически недоступна растениям до разрушения этих минералов с высвобождением калия в усвояемую растениями форму 30кг/га в год (Пчелкин, 1977). По-видимому, разрушение почвенных минералов усиливается на фоне удобрений и под хорошо развитым растительным покровом. Этому способствует попеременное увлажнение и высыхание почвы.
Рисунок. Формы калия в почве и их трансформация (Krauss, 1998)
Водно-растворимый калий наиболее подвижен и доступен растениям. Представлен легкорастворимыми его солями, находящимися в почвенном растворе. Его количество в зависимости от внешних условий постоянно меняется и составляет 1/5- 1/10 часть от обменного калия (1-7мг/кг почвы). Эта форма калия пополняется за счет гидролиза калийсодержащих минералов, разрушения их корневыми выделениями и продуктами жизнедеятельности почвенных микроорганизмов, но главным образом за счет вытеснения обменного калия. Растения могут усваивать до 50-70% водно-растворимого и обменного калия.
Калий органического вещества почвы представляет собой ту часть, которая входит непосредственно в состав гумуса, внесенных органических удобрений, растительных остатков, а также микробных тел. Этот калий становится доступным растениям лишь после отмирания микробных тел и минерализации источников органического вещества.
Обменный, или поглощенный калий составляет 0,8-1,5% . Представлен катионами калия в почвенном поглощающем комплексе. Вместе с водорастворимым калием это основной источник калийного питания растений. Но растения могут усваивать только какую-то часть всего запаса обменного калия, наиболее подвижную. Она вытесняется в почвенный раствор другими катионами, находящимися на поверхности корневых волосков растений.
Фиксация калия в необменном состоянии характерна для почв, богатых глинистыми минералами со сложной, трехслойной кристаллической решеткой. Этот калий внедряется в межпакетное пространство кристаллической решетки. Фиксация калия, при которой он вовлекается внутрь кристаллической решетки, усиливается при попеременном увлажнении и высыхании почвы, значительном содержании органического вещества почвы и щелочной реакции почвенного раствора.
Таким образом, калийное состояние почв связано со способностью катионов переходить из одной формы в другую. Эти превращения заключаются в возможности ионов калия занимать различные по прочности связи с почвой позиции, и относится к двум противоположно направленным, обратимым процессам фиксации (адсорбции) и мобилизации и (десорбции). Под фиксацией калия понимают переход катионов, находящихся в почвенном растворе или в обменном состоянии в необменную (прочносвязанную) форму. Поэтому, фиксацию калия можно рассматривать как процесс, ответственный за его накопление и сохранение. Десорбционная способность контролирует механизм удаления-потребления почвенного калия. Представляет процесс перехода катионов из обменно-поглощенного или необменного состояния в почвенный раствор.
10. Баланс калия
Баланс калия в агроценозах формируется из приходной и расходной частей. Приходная часть состоит из калия, поступающего из почвообразующих пород и минералов, зольного калия, калия плазмы микроорганизмов и с поступающими минеральными и органическими удобрениями. Расходная часть слагается калием, отчуждаемым из агроценоза с растительной продукцией, потери с поверхностным стоком, за счет инфильтрации и в виде необменной фиксации калия минералами.
Приходные статьи баланса калия
Все калийсодержащие минералы могут служить непосредственными источниками калийного питания растений. Доступность калия слюд и гидрослюд значительно выше. Коэффициент использования калия из слюд (мусковит, биотит, флогопит) составляет 39%, причем они хорошо обеспечивали растения калием при размере фракций от илистой до песчаной (Важенин, Карасева,1959, Петербургский, Кузнецов, 1972). Глинистые минералы (иллит, глауконит) могут быть использованы в качестве калийных удобрений (Грим,1967). По доступности калия растениям из минералов имеется следующий убывающий ряд: биотит-нефелиновая порода > мусковит > полевые шпаты (ортоклаз, микроклин).
Количество высвобождаемого калия зависит не только от общего количества конкретного минерала, но и от содержания в нем калия, зависящего от степени выветренности.
Таким образом, определенные количества разных минералов могут обеспечить одинаковое общее количество калия в субстрате, но условия калийного питания растений при этом будут совершенно различными. Доступность растениям калия определяется, прежде всего, прочностью его связи с минеральной основой почвы. Позиции, занимаемые ионами калия в его почвенных носителях, по возрастанию степени энергии связи можно классифицировать следующим образом:
а) калий, адсорбированный на минеральных и органоминеральных коллоидных частицах ППК. Обменные катионы удерживаются вокруг внешних краев кремнезем-глиноземных элементов структурных слоев глинистых минералов с различной энергией, которая зависит от положения адсорбированного катиона на поверхности минерала, концентрации ионов.
б) калий, необменно-поглощенный межслоевым пространством почвенных минералов с расширяющимся типом решетки (монтмориллонитового типа). Поглощенные катионы, проникающие между силикатными слоями этих минералов, переходят в менее подвижную, по сравнению с обменной, форму при сжимании решетки (Горбунов,1965). Данная реакция, как правило, обратима – при гидратировании коллоидов катионы могут снова переходить в раствор;
в) калий, расположенный в межплоскостном пространстве глинистых минералов с ненабухающей решеткой (гидрослюды). Ионы калия уравновешивают дефицит заряда, вызванный изоморфными замещениями внутри кристаллической решетки, и, поэтому удерживаются электростатическими силами достаточно прочно (Грим,1967);
г) калий, входящий в кристаллическую решетку минералов с листовой решеткой (слюд);
д) калий минералов с каркасным типом кристаллической решетки (полевых шпатов).
Таким образом, максимальной подвижностью обладают ионы почвенного раствора, минимальной – калий, входящий в каркасную кристаллическую решетку полевых шпатов.
Калий, поглощенный органической частью почвы (микробами, органическими остатками и гумифицированным веществом) составляет весьма небольшое количество. В составе золы гуминовой кислоты калий составляет 1,22%. Калий, входящий в состав плазмы микроорганизмов, густо населяющих почву и ризосферу, становится доступным лишь после отмирания микробов.
Калий в почвах малоподвижен – перемещение ионов калия за вегетационный период не превышает 3-7мм. Это делает возможным обогащение почвы калием внесением удобрений в запас, т.е. раз в 3-5 лет.
Расходные статьи баланса калия.
Вынос урожаями представляется основной расходной статьей баланса этого элемента питания. Ежегодно с урожаями технических, пропашных культур выносится более 110 кг/га калия. Считается, что растения предпочтительнее поглощают калий почвы, чем из свежевнесенного удобрения.
По литературным данным, содержание калия в зерне пшеницы является стабильным показателем и составляет 0,5- 0,6% (на сухое вещество); в соломе его уровень колеблется в более широких пределах – 0,8 -1,3%, а при внесении удобрений содержание калия в соломе пшеницы достигало 1,-3,8%.
Значительно варьирует содержание калия в клубнях картофеля, оно составляет от 0,67 до 2,7%. Еще более заметно колеблется концентрация элемента в картофельной ботве – 0,7 -3,8%.
Сельскохозяйственные культуры предъявляют неодинаковые требования к уровню калийного питания. Уровень калийного питания определяется динамикой и интенсивностью потребления элемента в течение вегетации. По этим показателям сельскохозяйственные растения подразделяются на 2 группы:
а) высокотребовательные к уровню калийного питания и отзывчивые на высокие дозы калийных удобрений – картофель, сахарная свекла, ячмень, подсолнечник, гречиха, просо, капуста, морковь, огурец, баклажаны, петрушка, сельдерей.
б) культуры с нормальной потребностью в калии, положительно отзывающиеся на последействие калийных удобрений, внесенных в высоких дозах под предшественник.
Вынос этого элемента с урожаем в интенсивных агроценозах может составлять 110 – 120 кг/га за счет почвенных запасов и 300 кг/га – при внесении калийных удобрений. Вынос калия капустой достигает 500 кг/га, томатом -220, морковью и картофелем -300, ячменем -400, пшеницей -200 кг/га.
Удельный вынос калия в целом увеличивается с повышением уровня калийного питания, но в значительной степени зависит от биологических особенностей выращиваемых культур. У культур с высоким потреблением калия его вынос возрастает по мере повышения доз удобрений. Растения с относительно низкой потребностью в калии склонны накапливать этот элемент в биомассе без соответствующего повышения продуктивности. В общем выносе калия на долю основной продукции приходится (в %): капуста и томат -70, морковь -75, картофель -80, пшеница и ячмень – 15.
Д.Н.Прянишников считал, что выносимое с урожаем количество калия должно быть компенсировано удобрениями не менее чем на 70-80%.
Минералогический и органо-минеральный состав почвы определяет такое ее важное свойство как способность фиксировать, или поглощать калий. Фиксация калия возрастает при высушивании почвы. Иногда фиксированный калий удерживается так прочно, что становится недоступным для растений. По данным С.М.Горбачевой (1977), в Красноярском крае необменная фиксация калия приводит к потере на черноземных, лугово-черноземных и серых лесных почвах до 60%, на серых лесных почвах – 25% элемента. Причем, фиксация проявляется при пониженной влажности и в условиях переменного избыточного увлажнения и последующего высушивания почвы
При водной и ветровой эрозии из корнеобитаемого слоя почвы теряется до 10% калия (обменного и водорастворимого).
- Какие вы знаете статьи расхода и прихода азота в почве?
- Значение биологического азота в обеспечении потребности возделываемых культур.
- Перечислите условия для поглощения аммиачного азота.
- Сущность денитрификации соединений азота.
- Роль азота в земледелии в свете учения Д.Н.Прянишникова.
- В какие органические соединения входит азот в растениях, какова их роль?
- Какие вы знаете источники азотного питания и как они превращаются в растениях?
- В чем особенности азотного питания бобовых культур?
- Расскажите о схеме превращения органических азотсодержащих веществ в почве. Что такое аммонификация и нитрификация?
- Какова роль фосфора в жизни растительного организма?
- В виде каких соединений находится фосфор в почвах и какова их доступность для растений?
- Содержание и формы фосфора в почве.
- Методы определения подвижных фосфатов почвы.
- Факторы, определяющие доступность почвенных фосфатов.
- Перечислите статьи прихода и расходования фосфора
- Какова роль калия в растениях?
- Каково валовое содержание калия в разных почвах?
- На какие группы подразделяются соединения калия в почвах и какова их доступность?
- Потребность сельскохозяйственных культур в калии.
- Зависимость содержания калия в почве от гранулометрического состава.
- Различия сельскохозяйственных культур в способности усвоения калия.
Желтая кукуруза, бледный подсолнечник и соя… Такую картину можно часто наблюдать на некоторых полях. Причины этому могут быть разные, но одна из основных – недостаток азота. Как правильно вносить азотные удобрения? Какие особенности внесения в технологии ноу-тилл? Когда лучше вносить азотные удобрения под яровые культуры? Какие есть методики и опасности? Об этом пойдет речь в этой статье.
ЦЕНА ВОПРОСА
Неправильное внесение азотных удобрений – деньги на ветер. И деньги немалые! К применению удобрений надо подходить ответственно, особенно азотсодержащих. Не стоит принимать решение только потому, что «вам так кажется» или «сосед так делает». Следует понимать принципы и нюансы применения азотных удобрений в технологии ноу-тилл.
 Азот внесенный неправильно — выброшенные деньги.
Азот внесенный неправильно — выброшенные деньги.
Неграмотное применение азотных удобрений приводит к прямым финансовым потерям, в виде затрат на удобрения и их внесение. Последствия могут быть разные: промывание, азотное голодание растений. В случае промывания загрязняется окружающая вас среда – нитраты попадают в ставки, реки и озера. Потери азота в результате промывания приведут к недобору урожая. А потом агроном с собственником будут гадать, что ж кукуруза в этом году не уродила?!
На сегодняшний день достаточно остро стоит вопрос внесения азотных удобрений под яровые культуры. Когда их лучше вносить? Осенью, весной или непосредственно перед посевом? Или дробно — осенью и весной? А не промоет влагой, то, что внесли осенью? Эти вопросы аграриев понятны – никто не хочет потратить деньги и не получить желаемого результата.
Чтобы получить ответы на эти вопросы нужно разобраться с формами азота, которые содержатся в популярных азотных удобрениях.
|
АЗОТ ВАЖЕН И ПОДВИЖЕН. БУДЬТЕ ОСТОРОЖНЫ! |
ФОРМЫ АЗОТА
Все знают про три формы азота: амидную NH2, аммонийную NH4 и нитратную NO3. Чем они отличаются?
Амидная форма усваивается только через листья. За 1-4 дня она превращается в аммонийную. Если удобрение содержит NH4 (аммонийную форму азота), то азот сразу же соединяется с почвой.
Аммонийная форма азота не промывается, но недоступна растениям. Чтобы азот NH4 стал доступен растениям, должен пройти процесс нитрификации, т.е. бактерии должны превратить его в NO3 – нитратную форму азота.
Для превращения аммонийной в нитратную форму необходимо от 7 до 40 дней, в зависимости от температуры. Процесс перехода из одной формы в другую можно выразить так:

Только нитратная форма усваивается растениями через корневую систему. Эта форма азота усваивается сразу после внесения. NO3 никогда не связывается с почвой, и поэтому может промываться. Особенно это проявляется на песчаных почвах и склонах. Нитратная форма азота доступна растениям, и может усваиваться даже при низких температурах.
|
ЧЕРЕЗ КОРНИ РАСТЕНИЯ УСВАИВАЮТ ТОЛЬКО НИТРАТНУЮ ФОРМУ АЗОТА |
КАРБАМИД, СЕЛИТРА или КАС?
Карбамид содержит одну форму азота – амидную. Как мы уже отмечали, эта форма усваивается только через листовую поверхность. Для превращения в доступную нитратную форму может понадобится 40-45 дней и температура не ниже +5…+10°С. В холодное время года карбамид неэффективен. Азот, который содержится в карбамиде, будет доступен растению только после преобразования в нитратную форму.
Карбамид — не лучший выбор основного азотного удобрения для Ноу-тилл. Амидная форма азота будет работать только на будущий урожай. А ноутильщику интересно еще и разложение растительных остатков.

Аммиачная селитра содержит две формы азота – аммонийную NH4 и нитратную NO3. Одна из них «подвижная» и может промываться, другая — закрепляется в почве и постепенно трансформируется в «подвижную» и доступную. Этот вид удобрений рекомендуется вносить на влажную почву при температуре НЕ выше +10°С .
Селитру можно закупить заранее и хранить в хозяйстве. Это дает безусловную оперативность для внесения. Вносить селитру можно разбрасывателем, что дает хорошую равномерность распределения.
КАС (карбамидно-аммиачная смесь) – содержит все три формы азота. Нитратная форма азота, которая содержится в КАС, сразу же доступна растениям, в то время как две остальные — амидная и аммонийная – постепенно трансформируются в нитратную.
Селитра и КАС содержат нитратную форму, которая и будет служить “пищей” для бактерий и грибов, которые минерализуют растительные остатки.
Следует отметить, что КАС не требователен к условиям внесения. Ни температура, ни влажность почвы не влияют на возможные “потери” азота. Вносить КАС можно даже при высокой температуре и в сухую почву.
КАС имеет определенные ограничения при транспортировке и хранении. КАС чрезвычайно агрессивная жидкость. Не всякий опрыскиватель выдержит это испытание. Кроме того, при внесении трубки опрыскивателя могут забиваться мусоринками, что негативно отразится на равномерности внесения.
СКОЛЬКО И ДЛЯ ЧЕГО?
Азотные удобрения в технологии no-till вносятся не только на запланированный урожай, но и на разложение растительных остатков.
Минерализация (разложение) растительных остатков происходит за счет грибов и бактерий. Эти микроорганизмы живут в почве и на поверхности. Они сохраняют активность при благоприятных условиях: температура +5…+40°С и наличие влаги. Для развития грибов и бактерий, и поддержания их жизнедеятельности нужны органическая масса (растительные остатки) и азот. О том как мы рассчитываем количество удобрений в своих хозяйствах — уже писалось ранее (отрывок статьи ниже).

Если не дать дополнительного азота на разложение растительных остатков, то микроорганизмы в любом случае будут потреблять азот из почвы, который был предназначен для растений. Если не учитывать это при расчете нормы азотных удобрений, то результатом станет снижение урожайности.
Кстати — это одна из так называемых “детских ошибок” начинающих ноутильщиков. Результат такого подхода можно увидеть на фотографии, где видна граница между соей, посеянной по овсу (справа) и соей, посеянной по кукурузе (слева).
 При внесении азотных удобрений не была учтена разница в количестве растительных остатков.
При внесении азотных удобрений не была учтена разница в количестве растительных остатков.
|
УЧИТЫВАЙТЕ КОЛИЧЕСТВО РАСТИТЕЛЬНЫХ ОСТАТКОВ НА ПОЛЕ |
КОГДА ВНОСИТЬ АЗОТНЫЕ УДОБРЕНИЯ?
В технологии Ноу-тилл азотные удобрения вносятся на поверхность почвы. По сути, так же как и в любой другой технологии. Азотные удобрения под посев яровых культур можно вносить и осенью, и весной. Все зависит от условий, в которых находится хозяйство: количество осадков, типы почвы, рельеф местности, температурных режим.
В регионах с достаточным количеством осадков и песчаными почвами возможно промывание азота. Поэтому внесение удобрений, содержащих форму NO3 лучше проводить ближе к посеву, т.е. в весенний период.
На равнинных черноземных почвах, при среднегодовой норме осадков не более 350 мм, азотные удобрения под яровые культуры можно вносить поздней осенью. Конкретнее – с конца октября до появления снежного покрова.
По снежному покрову вносить удобрения не стоит. Некоторые фермеры считают, что если снежный покров несущественный (до 5 см), то можно вносить азотные удобрения. Это ошибка! Даже при тонком снежном покрове малейшее таяние снега вызовет сток воды. Вода будет перемещать азот в низины, которые есть на каждом поле. Это приведет к неравномерному распределению азота на поле.
На полях со cклонами всегда будут смывы и промывание. А при достаточном количестве осадков потери азота неизбежны и огромны!
Поздней осенью, как правило, создаются идеальные условия для внесения аммиачной селитры. Почва в этот период влажная, а температура воздуха и почвы не превышает +10°С. При такой температуре азот не «улетает».
Весной температура воздуха растет. Верхний слой почвы теряет влагу. Окно для эффективного внесения азотных удобрений крайне небольшое. Это происходит не только по погодным условиям, но и потому, что в этот период накладывается еще одна операция в поле — идет подкормка озимых рапса и пшеницы. Поэтому, необходимо «ловить» мерзло-талую почву.
Таким образом , мы выяснили, что лучший эффект дают азотные удобрения, которые содержат две и более форм азота. При внесении следует учитывать количество осадков в регионе, тип почвы и наличие склонов на полях. Расчет нормы нужно делать с учетом количества азота, необходимого для разложения растительных остатков культуры-предшественника. Гранулированные азотные удобрения максимально эффективны, если вносятся на влажную почву.
Как вносят азотные удобрения в хозяйствах “Компании Агромир”? Везде применяется аммиачная селитра. В хозяйствах Кировоградской области внесение обычно планируется на осень. Случается и весеннее внесение. Опыт показал, что время внесения удобрений не влияет на урожайность. Хотя, некоторые специалисты считают, что осеннее внесение предпочтительнее.
В Житомирской и Тернопольской областях разбрасывание аммиачной селитры производится весной. Причина уже рассматривалась выше: склоновые поля, обильные осадки и песчаные почвы.
Понимание правил и зависимостей, которые были изложены в данной статье, позволит вам максимально эффективно использовать азотные удобрения.
Выбирайте формы, рассчитывайте нормы и вносите азотные удобрения правильно. Темно зеленых вам посевов и высоких урожаев.
Хотите узнать больше о Ноу-Тилл технологии — подпишитесь на
Чтобы задать вопрос или оставить отзыв -
нажмите сюда
Современный ассортимент азотных минеральных удобрений, выпускаемых промышленностью, делятся на шесть групп: аммиачные, аммонийные, нитратные, аммонийно-нитратные, амидные и аммиакаты. В отдельную группу выделяют азотные удобрения длительного действия.
Производство азотных удобрений основывается преимущественно на использовании синтетического аммиака. Прямое связывание азота в виде его оксидов и цианамида кальция стоит значительно дороже и используется редко. Источником азота является атмосфера. Водород для синтеза аммиака добывают из газа при коксования угля, из воды в результате разложения в процессе га-зификации твердого топлива и мазута, при переработке углеводородных газов (природного, попутного) конверсией с водяным паром, а также во время электролиза воды. Чаще всего для получения водорода используют природные и попутные нефтяные газы.
Синтетический аммиак добывают при взаимодействии химически чистых азота и водорода в соотношении 1: 3. Для этого добытую смесь с помощью компрессоров сначала постепенно сжимают, а затем подают в контактную печь (камеру синтеза), где при высокой температуре (400-500 ° С) и наличии катализаторов (железа с добавками оксидов алюминия и калия) происходит синтез аммиака:
N2 + ЗН2 = 2NH3.
Затем аммиак поступает в холодильник и сжижается. Таким образом, стоимость азотных удобрений во многом зависит от стоимости энергии. Сейчас аммиак является почти единственным источником связанного азота, который используют для получения различных форм азотных удобрений. По оценке ученых, изучающих азотные циклы в природе, не менее 40% населения Земли живет только благодаря открытию синтеза аммиака. Внести такое количество азота в почву с органическими удобрениями невозможно, даже если бы все человечество этим занималось. Современное отечественное производство азотных удобрений соответствует международным стандартам. Основными твердыми азотными удобрениями является аммиачная селитра и карбамид. Увеличиваются поставки безводного аммиака и растворов нитрата аммония и карбамида (КАС). Количества некоторых форм азотных удобрений (натриевая и кальциевая селитры, сульфат аммония, аммиачная вода) в перспективе не будут превышать нескольких процентов всех поставок азота.
Аммиачные удобрения
К этой группе азотных удобрений относятся удобрения, содержащие азот в аммиачной форме (NH3). Это жидкий (безводный) и водный аммиак (или аммиачная вода).
Аммиак жидкий NH3 (аммиак жидкий безводный, аммиак сжиженный, охлажденный аммиак) - найконцентрованише и дешевое азотное удобрение, содержащее 82,3% азота, остальное - водород. Это удобрение является сжиженным под давлением 1,6 МПа при температуре 40 ° С газом. По внешним признакам - бесцветная летучая жидкость с характерным резким запахом. Во время охлаждения до температуры - 33,3 ° С аммиак сжижается, а при температуре -77,7 ° С затвердевает и превращается в снегообразную массу. С повышением давления аммиак переходит в жидкое состояние даже при комнатной температуре, поэтому его хранят и перевозят в специальных толстостенных стальных цистернах или баллонах, выдерживающие давление 2-3 МПа. Плотность сжиженного аммиака при температуре 20 ° С составляет 0,61 г / см3, температура кипения 34 ° С. Это сильнодействующее ядовитое вещество, смесь которой с воздухом при объемной концентрации аммиака 15-27% может взрываться даже от искры. В случае попадания на кожу жидкий аммиак вызывает ожоги, а в случае испарения - обморожения. При вдыхании воздуха, содержащего аммиак в соотношении 1: 10000, наступает смерть.
Если емкостей для хранения жидкого аммиака нет, то из него изготавливают аммиачную воду. Для этого жидкий аммиак пропускают сквозь чистую воду в специально оборудованных резервуарах.
Жидкий аммиак вносят в почву осенью или весной специальными машинами. В почве аммиак поглощается почвенным раствором, абсорбируется его коллоидами и не вымывается. При этом выделяется гидроксид аммония, который взаимодействует с анионами почвенного раствора с образованием различных солей. Аммиак краше закрепляется на тяжелых и суглинистых почвах с умеренной их влажности (50-60 % полной влагоемкости). При таких условиях супесчаные почвы могут содержать 1600, суглинистые - 2700 кг аммиака на 1 га. Потери аммиака при этом составляют около 1,5 %.
В случае внесения в сухой или очень переувлажненный почву потери аммиака увеличиваются, в частности за неглубокого зарабатывания и на почвах легкого гранулометрического состава. Поэтому важно правильно установить глубину внесения жидких азотных удобрений.
Наряду с физико-химическими реакциями в почве происходят процессы нитрификации аммиака. Скорость и степень поглощения аммиака почвой, а также его газообразные потери зависят от глубины внесения в почву, его гранулометрического состава, влажности и содержания гумуса. Сжиженный аммиак на почвах тяжелого и среднего гранулометрического состава вносят на глубину 10-12 см. На легких почвах это удобрение сохраняется дольше в виде NH3, поэтому возможны его газообразные потери; глубина внесения должна быть не менее 14-16 см. На недостаточно обработанных участках, переувлажненных или сухих почвах, а также после известкования глубину внесения аммиака увеличивают на 3-5 см.
В первые дни после внесения жидкого аммиака равновесие реакции почвы сначала смещается в сторону ощелачивания к pH 9, а затем, вследствие нитрификации аммонийного азота, в сторону подкисления. В зоне внесения аммиака происходит временная стерилизация почвы и нитрификация прекращается. Однако уже через 1-2 недели количество микроорганизмов в почве восстанавливается и в результате лучшего азотного питания в дальнейшем превышает начальный уровень. В оптимальных условиях процесс полной нитрификации аммиака завершается в течение месяца. Это способствует снижению pH почвенного раствора, поэтому удобрение будет физиологически кислую реакцию. Колебания pH положительно влияет на доступность для растений фосфатов и микроэлементов почвы. Внесение аммиака в корнеобитаемом слой почвы может привести к частичному разрушению корневых волосков и тканей корня. Его негативное воздействие оказывается до тех пор, пока он не превратится в аммоний. Продолжается это от нескольких часов до 10-15 суток, а затем аммоний начинает поглощаться корневой системой растений. Количество поглощенного аммония зависит от грунтовых и погодных условий, поэтому жидкий аммиак желательно вносить до посева сельскохозяйственных культур.
В сельском хозяйстве жидкий аммиак используют также для аммонизации грубых кормов, торфа, обезжиривание жидкого навоза и др.
Агрохимическая оценка аммиака практически равноценна, а в некоторых случаях вуза за эквивалентное количество азота, внесенное с твердыми азотными удобрениями. Себестоимость единицы азота в аммиаке примерно на 1/3 ниже, чем в самом дешевом твердом азотном удобрении - аммиачной селитре, возможна полная механизация - от транспортировки до внесения в почву. Кроме того, жидкий аммиак, как и другие жидкие удобрения, не имеет таких негативных свойств твердых удобрений, как слеживания, сегрегация и тому подобное. Ценность этого удобрения снижается из-за высоких затрат на технику, а также ограниченность применения.
Аммиак водный технический (аммиак водный, аммиачная вода) NH3 + NH4OH + Н2О - раствор аммиака в воде (в одном объеме воды растворяется около 700 объемов аммиака). В удобрении аммиака значительно больше, чем аммония. Потери азота при его перевозке, хранении и внесении связанные с выветривания аммиака. В концентрированном растворе содержится 20,5% азота (в пересчете на NH3 - 25%), его плотность при этом равна 0,91 г / см3. В таком состоянии его и поставляют сельскому хозяйству. Это прозрачная жидкость, которая иногда имеет желтоватый цвет. Допускается изготовление аммиачной воды летом (май-август) с содержанием аммиака не менее 22% (в пересчете на азот - не менее 18%). Содержание азота в аммиачной воде контролируют с помощью ареометра, поскольку с изменением концентрации аммиака меняется плотность раствора.
Удобрение имеет невысокое давление пара, а не корродирует черные металлы. При содержании 20% раствор аммиака замерзает при температуре - 33 ° С, при содержании 25% - при температуре - 50 ° С. Это позволяет перевозить и хранить его в герметичных резервуарах из обычной углеродистой стали, оборудованных специальными предохранительными клапанами, которые рассчитаны на давление 150-200 кПа. Из воды аммиак испаряется в 5-6 раз быстрее, чем бензин. Для уменьшения потерь азота при хранении в резервуары добавляют специальную герметизационных самозатичну пленкообразующее смесь. Аммиачная вода, как и жидкий аммиак, корродирует цветные металлы (медь, цинк, олово) и их сплавы (бронзу, латунь). Поэтому насосы, краны и клапаны изготавливаются из черных металлов или чугуна. Алюминий и резина этими удобрениями не поражаются.
Наличие в аммиачной воде большого количества свободного аммиака требует внесения ее, как и жидкого аммиака, непосредственно на глубину 10-12 см на глинистых и 12-15 см на супесчаных почвах.
На глинистых почвах аммиачную воду, как и безводный аммиак, можно вносить и осенью почти под все культуры, когда температура почвы снижается до 10 ° С и ниже, и весной перед посевом и для подкормки пропашных культур (свекла, кукуруза, подсолнечник). На почвах легкого гранулометрического состава это удобрение рекомендуется вносить весной.
Для культур сплошного сева расстояние между лапами культиватора (наконечниками) при внесении аммиачной воды должно быть 20-25 см, для пропашных - равняться ширине одного междурядья.
При внесении жидких азотных удобрений следует помнить, что это сильные щелочи, которые повреждают живые ткани при попадании на их поверхность.
Применение аммиачной воды и жидкого аммиака на всех почвах приводит частичную стерилизацию, так погибают насекомые, черви, личинки проволочника и другие организмы, населяющие почву. В местах внесения аммиака сначала снижается количество грибов, бактерий, актиномицетов. Микроорганизмы, которые лучше переносят повышенную концентрацию аммиака и слабощелочной реакции, через 5-10 суток восстанавливают свою жизнедеятельность и активность. По данным В. В. Эндрюса и других ученых, количество бактерий и актиномицетов через несколько суток после внесения жидких азотных удобрений увеличивается в 25 раз.
Аммиачная вода сначала угнетает нитрификувальни бактерии, но через 5 дней их количество увеличивается в 10 раз. В некоторых случаях это положительное явление. Например, за внесение аммиачных удобрений осенью в условиях теплой и влажной погоды ослабление нитрификацийнои способности снижает потери нитратного азота в результате вымывания.
Аммиачные удобрения положительно влияют на корневую микрофлору. В ней увеличивается количество аммонификаторов и нитрификаторов, а количество денитрификатор уменьшается в 10 раз.
Производство аммиачной воды по сравнению с производством твердых удобрений на 30-40% дешевле, поскольку отпадают такие технологические операции как гранулирования, сушки, сортировки и кондиционирования продукта. Стоимость единицы действующего вещества в аммиачной воде в 1,5-2 раза ниже, чем в аммиачной селитре. Кроме того, в 2-3 раза сокращаются затраты труда на внесение аммиачной воды, поскольку она не требует подготовки удобрений для внесения, поскольку все операции по ее использованию (погрузка, выгрузка, внесение) полностью механизированы.
Азот - он же в таблице Менделеева N (он же - первая буква в аббревиатуре NPK на многочисленных упаковках с удобрениями).
Прежде чем подробно разобрать роль и формы азота в удобрениях, нужно напомнить, что он относится к группе МАКРОэлементов . Это категория жизненно необходимых абсолютно всем растениям элементов, куда помимо азота входит фосфор P и калий K. МИКРОэлементы (железо, сера, цинк, марганец и другие) также играют важную роль, но они необходимы в дозировках в сотни раз меньше, чем макроэлементы (отсюда и название «микро»). Азот как и фосфор и калий напрямую участвуют в формировании основных тканей растения, отвечают за фазы развития (рост, вегетация, цветение, плодоношение) и скорость роста.
Зачем растению азот?
Если бы художник захотел нарисовать картинку благоухающего сада из элементов таблицы Менделеева, то вместо зелени листвы, стеблей и молодых побегов была бы буква N - азот. Именно этот летучий газ участвует через различные соединения в формировании хлорофилла - того самого белка, который принимает участие в фотосинтезе и дыхании растения. Если азота достаточно - листва имеет насыщенный изумрудный цвет, который вкупе с хорошим поливом может отливать глянцем. Как только азота становится мало, растение бледнеет вплоть до чахлой желтизны, а новые побеги растут медленно или практически прекращают рост. НА ФОТО:
Разница между растениями, получавшими азот в процессе выращивания и теми, что росли на бедных почвах - очевидна
НА ФОТО:
Разница между растениями, получавшими азот в процессе выращивания и теми, что росли на бедных почвах - очевидна
Также принято считать, что за плодоношение отвечает фосфор, и именно его присутствие будет влиять на урожай. Это действительно так, но в большей степени в вопросе качества урожая. За количество будет отвечать азот. Чем больше вегетативной массы наберет растение, тем больше цветочных почек появится на стеблях или в пазухах. У некоторых растений азот напрямую влияет на формирование цветочных почек, особенно у двудомных с женскими и мужскими цветками (конопля, ива, лимонник, облепиха и многие другие).
Как понять, что растению не хватает азота?
Первый признак нехватки азота - чахлый, желтушный, вплоть до бледно-желтого, цвет листвы. Пожелтение начинается с краев листа по направлению к центру. При этом листовая пластинка утончается, становится мягкой, даже если соблюдается полив. Очень похожие симптомы наблюдаются при нехватке серы (S), однако в случае с азотом нижние листья желтеют первыми. В запущенных случаях они высыхают и опадают - растение «вытягивает» все питательные вещества из них, чтобы отдать верхним побегам или плодам, если они имеются. При нехватке серы опадения листвы снизу не наблюдается.
Причин нехватки может быть, как правило, две: или растение забыли подкормить (когда и как подкармливать - ниже) или грунт сильно закислен, и кислая реакция среды нарушает всасываемость азота. Также в кислой среде нехватка азота может мимикрировать под хлороз - недостаток железа или магния. Однако в данном случае это непринципиально - грунт требует решительной замены или обновления.
Какой азот продают в магазинах и какой из них лучше?
Для каждого садовода этот вопрос, пожалуй, самый главный. Однако давайте для начала разберемся, а какой в принципе азот бывает? Без этого будет трудно понять, что написано на упаковке.
Аммиачный или аммонийный азот (NH 4)
Этот азот еще называют органическим азотом. Его действительно много в органических остатках разлагающегося вещества будто то навоз или опавшая листва. Растения очень любят аммоний, так как он легко проникает в корни и в них же может превращаться с аминокислоты, которые и будут формировать листья и побеги растения. Однако есть существенный минус: несмотря на все механизмы сопротивления, аммоний может проникать в клетку растения и оказывать на нее токсичный эффект.
В природе передозировка аммонием довольно редка, т.к. он довольно быстро «преобразуется» бактериями до нитратов NO 3 (процесс нитрификации) и далее до нитритов (NO 2) и вплоть до чистого азота, который быстро улетучивается из почвы. В саду или огороде аммиачный азот также быстро покидает почву, если только владелец участка не применил чистый, свежий навоз в большом количестве. В этом случае и происходит т.н. «сжигание» корней или всего растения. В комнатных условиях органический азот следует использовать по-минимуму, т.к. проконтролировать нужную дозировку довольно сложно.
ВАЖНО : на упаковках удобрений для комнатных растений аммиачный азот крайне редко указывается формулой (NH 4) или формулировкой. Как правило, используется органическая форма: некий экстракт (например, экстракт водорослей) или жидкая форма чистого органического удобрения («биогумус»), или гелеобразная масса («сапропель» - донный ил) и т.д.

Для сада и огорода применяется минеральная форма - сульфат аммония (NH 4) 2 SO 4 . Большое преимущество этого удобрения в том, что оно также содержит серу. Вместе с азотом она участвует в синтезе важных аминокислот, включая незаменимые. Сульфат аммония входит в состав популярной сегодня марки удобрения «Акварин» (номера 6 и 7 подходят для сада и огорода). Это удобрение содержит приблизительно 25% аммонийного и 75% нитратного азота.
Нитратный азот (NO 3)
Если органический азот растение старается сразу пустить в дело, не затрачивая энергии, то с нитратом картина совершенно противоположная. Практически любая культура жадно запасает нитраты в тканях в количествах порой превышающих допустимые пределы! А всему виной - высокая подвижность азота в биосфере. Сегодня коровка плюхнула лепешку, на нее тут же набрасываются бактерии (а чуть позже и насекомые), которые переводят азот из органической в минеральную форму NO 3 . Но и эта форма долго не задерживается: то, что не успели забрать растения, уже другие бактерии доводят до нитритной NO 2 формы, а потом и до азота. Плюс нитрата - безвредность для растения. Минус - необходимость света и тепла, благодаря которым нитрат в листьях восстанавливается до аммония (точнее различных аминов NH 2) и далее - до аминокислот и белков. Как итог: в неблагоприятных условиях растение будет стремиться накапливать нитраты, чтобы использовать их, когда ситуация наладится.
В комнатных условиях нитратный азот - настоящее решение. Он указывается формулой на упаковке NO 3 и сопровождается соответствующим текстом. Дозировки рассчитаны заранее для периодов покоя и активного роста. Ошибиться невозможно.
 В саду и огороде
нитратный азот используется сразу
после начала сокодвижения (что соответствует температуре почвы около +15°С). Важно не упустить этот момент и обеспечить растение элементом, из которого уже в самые ближайшие дни начнут строиться новые побеги и листья. Заканчивают применение азотных удобрений в июле, а точнее - сразу после завершения периода вегетации (деревья и кустарники замедляют рост, начинается плодоношение). В зиму сад отправляют без азотной подкормки или делают это поздней осенью, перед заморозками и органической формой, которая задержится в почве подольше. Также не забываем, что зимы в последнее время теплеют, что не лучшим образом сказывается на удержании азота в почве.
В саду и огороде
нитратный азот используется сразу
после начала сокодвижения (что соответствует температуре почвы около +15°С). Важно не упустить этот момент и обеспечить растение элементом, из которого уже в самые ближайшие дни начнут строиться новые побеги и листья. Заканчивают применение азотных удобрений в июле, а точнее - сразу после завершения периода вегетации (деревья и кустарники замедляют рост, начинается плодоношение). В зиму сад отправляют без азотной подкормки или делают это поздней осенью, перед заморозками и органической формой, которая задержится в почве подольше. Также не забываем, что зимы в последнее время теплеют, что не лучшим образом сказывается на удержании азота в почве.
В обиходе нитратный азот известен как селитра , из которой наиболее популярна в России - калийная (или «калиевая») селитра. Эта форма нитратного азота подходит как для садовых, так и для комнатных растений. Обеспечивает легкоусвояемым азотом и калием.
Амидный азот CO(NH 2) 2 , карбамид или просто мочевина
Богатое, биогенное (то есть полученное в том числе органическим путем) удобрение, которое может содержать до 46% азота. Для использования в грунте в последнее время используется редко, т.к. вездесущие «уреазные» бактерии быстро переводят драгоценную мочевину в карбонат аммония более известный в пищевой промышленности как разрыхлитель теста. Вот таким «разрыхлителем» в советские годы «удобряли» поля, пока не осознали потери азота. Сегодня мочевина используется в растворах для опрыскивания. Разумеется, лучшее ее применение – на полях и в больших садах. В частной практике применяется редко, поэтому и на полках обычных магазинов практически не встречается.
Мочевина - прекрасное средство против парши и некоторых других патогенных грибков.
Подведем итог
- Азот - один из важнейших элементов, который постоянно необходим растению для здорового роста и развития.
- В комнатной культуре азотные удобрения добавляют в период активного роста. За месяц-полтора до покоя азотное питание прекращают, чтобы не вызвать избыточный рост и нарушение периода покоя.
- В садовой и огородной культуре азот добавляют весной, как только температура прогреется до +15°С (корни начинают впитывать влагу). Конец периода применения: середина лета; начало августа - только в случае холодной весны/лета.
- В комнатной культуре необходимо использовать нитратный азот: на упаковке будет написано NO 3 , возможно встретится только слово «нитрат».
- В садовой культуре, как правило, используются готовые марки удобрений, в которых смешаны нитратные и аммонийные формы азота. Оба указываются на упаковке формулами сульфата аммония и нитрата калия (чаще всего).
- Если вам попадется мочевина (карбамид), то используйте ее для опрыскивания растений. Период использования аналогичен другим формам азота.
Азотные удобрения - азотосодержащие вещества, которые используются для повышения содержания азота в почве. В зависимости от формы азотного соединения, однокомпонентные азотные удобрения подразделяются на шесть групп. Используются в основной прием как припосевные удобрения и в качестве . Производство основано на получении синтетического аммиака из молекулярного водорода и азота.
Показать все
Группы азотных удобрений
В зависимости от содержащегося азотного соединения, однокомпонентные азотные удобрения подразделяются на шесть групп:
- ( , );
- ( , хлористый аммоний);
- Амидные ();
- ( , (КАС);
Нитратные удобрения
Нитратные удобрения содержат в нитратной форме (NO 3 -). К этой группе относятся NaNO 3 и Ca(NO 3) 2 .
Нитратные удобрения являются физиологически щелочными и сдвигают реакцию почвы от кислой к нейтральной. В связи с этим свойством их использование очень эффективно на кислых дерново-подзолистых почвах. Не рекомендуется использование на засоленных почвах.
 Азотные удобрения (по формам азота)
Азотные удобрения (по формам азота)
Аммонийные удобрения - вещества, содержащие в форме катиона аммония NH 4 + .
К ним относятся сульфат аммония (NH 4) 2 SO 4 , сульфат аммония-натрия (NH 4) 2 SO+Na 2 SO 4 или Na(NH4)SO4*2H2O), хлористый аммоний NН 4 Сl.
Производство аммонийных удобрений проще и дешевле, чем нитратных, поскольку окисление аммиака в азотную кислоту не требуется.
во всем мире используют в орошаемом земледелии под рис и хлопчатник, особенно в районах избыточного увлажнения, в частности, в тропиках.В России сульфат аммония производят с 1899 года. Впервые его получили в Донбассе, на Щербинском руднике путем улавливания и нейтрализации серной кислотой аммиака, который образуется при коксовании каменного угля. Принципиальную схему этого способа используют и сейчас. получают как отход производства капролака. Эффективно при внесении под свеклу и другие корнеплоды из-за присутствия натрия. Рекомендуется для сенокосов и пастбищ.Хлористый аммоний (хлорид аммония)
содержит значительное количество хлора - 67 %, 24-26 %. Применять под чувствительные к хлору культуры (картофель, табак, виноград, лук, капусту, лен, коноплю) в качестве удобрения или не рекомендуется. Вносить хлорид аммония под хлорофобные культуры можно только осенью и в зонах достаточного увлажнения. В таком случае ионы хлора будут вымыты из корнеобитаемого слоя атмосферными осадками.Хлорид аммония - мелкокристаллический порошок желтоватого или белого цвета. При 20°C в 100 м 3 воды растворяется 37,2 г вещества. Обладает хорошими физическими свойствами, при хранении не слеживается, малогигроскопичен.
Хлорид аммония получают как побочный продукт при производстве соды.
Аммонийно-нитратные удобрения содержат азот в аммонийной (NH 4 +) и нитратной форме (NO 3 -). К этой группе причисляют аммиачную селитру (NH 4 NO 3), сульфо-нитрат аммония ((NH 4) 2 SO 4 *2NH 4 NO 3 +(NH 4)SO 4), известково-аммонийную селитру (NH 4 NO 3 *CaCO 3).
содержит нитратный и аммонийный азот в соотношении 1: 1. Правильнее называть это удобрение аммонийной селитрой, но аммиачная селитра - название более распространенное. Это наиболее эффективное из однокомпонентных азотных удобрений. Аммиачная селитра - безбалластное удобрение. Стоимость его перевозки и внесения в почву значительно ниже, чем у других азотных удобрений (исключение - мочевина и жидкий аммиак). Сочетание подвижного нитратного азота с менее подвижным аммонийным азотом дает возможность широкого варьирования способов, доз и сроков внесения аммиачной селитры в зависимости от региональных почвенно-климатических условий и особенностей агротехники выращивания культур. (сульфат-нитрат аммония, монтан-селитра, лейна-селитра) - сероватое мелкокристаллическое или гранулированное вещество сероватого цвета.Физико-химические свойства удобрения позволяют успешно использовать его в различных почвенно-климатических условиях. Обладает потенциальной кислотностью.
Известково-аммонийная селитра
- гранулированное удобрение. Соотношение селитры и извести варьирует в зависимости от марки удобрения. Широко используется в странах Западной Европы.Амидные удобрения
Амидные удобрения содержат в амидной форме (NH 2 -). К этой группе относится мочевина CO(NH 2) 2 . Азот в мочевине присутствует в органической форме в виде амида карбаминовой кислоты. Это наиболее распространенное твердое азотное удобрение. Применяется во все приемы внесения, но наиболее эффективно для .
Жидкие аммиачные удобрения - жидкие формы азотных удобрений. К этой группе относятся жидкий (безводный аммиак) NH 3 , аммиачная вода (водный аммиак), аммиакаты. Производство жидких аммиачных удобрений значительно дешевле, чем твердых солей.
содержит 82,3 % . Это самое концентрированное безбалластное удобрение. Внешне - бесцветная жидкость. Физико-химические свойства удобрения изменяются в зависимости от температуры окружающей среды. Хранится только в герметических сосудах, где под давлением разделяется на жидкую и газообразную фазы.При транспортировке емкости заполняют не полностью. Вещество нейтрально к чугуну, железу и стали, но сильно коррозирует цинк, медь и их сплавы.
- раствор аммиака в воде, давление паров невысокое, черные металлы не разрушает. Азот содержится в форме аммиака NH 3 и аммония NH 4 OH. Свободного аммиака содержится гораздо больше, чем аммония. Это способствует потерям азота за счет улетучивания. Работать с аммиачной водой проще и безопаснее, чем с безводным аммиаком, но в связи с низким содержанием азота ее применение рентабельно только в хозяйствах, расположенных недалеко от предприятий, ее производящих.Аммиакаты
содержат от 30 до 50 % азота. Внешне это жидкость светло-желтого или желтого цвета. Получают аммиакаты при растворении в водном аммиаке аммиачной селитры, аммиачной и кальциевой селитры, мочевины или аммиачной селитры и мочевины.Аммиакаты отличаются по концентрации общего азота, по соотношению его форм и разнообразны по физико-химическим свойствам.
Аммиакаты вызывают коррозию медных сплавов. Аммиакаты с аммиачной селитрой окисляют, кроме того, и черные металлы. Хранение и транспортировка аммиакатов возможны в емкостях из алюминия, его сплавов, нержавеющей стали или в обычных стальных цистернах с антикоррозийным покрытием эпоксидными смолами. Возможно применение емкостей из полимерных материалов.
(КАС)
- смесь водных растворов мочевины и аммиачной селитры. КАС обладают нейтральной или слабощелочной реакцией. Внешне - прозрачные либо желтоватые жидкости. Путем изменения соотношения исходных компонентов получают различные марки КАС.Поведение в почве
Все однокомпонентные азотные удобрения хорошо растворимы в воде.
Нитратные формы
передвигаются вместе с почвенным раствором и связываются в почве только биологическим типом поглощения. Биологическое поглощение активно только в теплое время года. С поздней осени до ранней весны нитраты легко передвигаются в почве и в условиях промывного водного режима могут вымываться, что особенно характерно для легких почв.В теплое время года в почвах преобладают восходящие потоки влаги. А растения и микроорганизмы активно поглощают нитратный азот.
Аммиачные и аммонийные
формы в почве поглощаются почвенным комплексом (ППК) и переходят в обменно-поглощенное состояние. В таком виде подвижность азота теряется, и он не вымывается. Исключение - легкие почвы с низкой емкостью поглощения.Дальнейшие процессы нитрификации способствуют трансформации азота в нитратные формы и биологическому поглощению его растениями и микроорганизмами почвы.
С мочевиной
после ее превращения под влиянием уробактерий в аммонийные формы азота происходит то же самое.Таким образом, азотные удобрения изначально или в процессе нитрификации скапливаются в почве в нитратной форме, которая впоследствии подвергается денитрификации. Эти процессы протекают практически во всех типах почв, и именно с ними связаны основные потери азота.
С агрономической точки зрения, денитрификация является негативным процессом. Но с экологической стороны она играет позитивную роль, поскольку освобождает почву от не использованных растениями нитратов и уменьшает их поступление в сточные воды и водоемы.
Применение на различных типах почв
Эффективность внесения азотных удобрений зависит от почвенно-климатических условий региона. Наибольшая эффективность азотных удобрений наблюдается в районах достаточного увлажнения.
Бедные гумусом дерново-подзолистые почвы, серые лесные почвы, оподзоленные, выщелоченные черноземы
. Действие азотных удобрений устойчиво положительно. Причем, с повышением степени выщелоченности черноземов возрастает и эффективность азотных удобрений.Супесчаные, песчаные почвы
нечерноземной зоны испытывают острую нехватку азота, поэтому здесь наблюдается высокая эффективность действия азотных удобрений. Однако в условиях промывного режима почвы отмечаются значительные потери азота, и его внесение производят преимущественно в весенний период.Осушенные торфяно-болотные почвы
. Действие азотных удобрений снижается, поскольку в минимуме оказываются фосфорные и калийные удобрения. Однако в первые годы освоения торфяников в центральных и северо-западных районах нечерноземной зоны возрастает и эффективность азотных удобрений.Оподзоленные и выщелоченные черноземы
правобережной лесостепи Украины показывают большую эффективность по применению азотных удобрений, чемлевобережной.Выщелоченные черноземы европейской части России
. Наблюдается меньшая эффективность азотных удобрений в Поволжье. В Центрально-Черноземной зоне и на Северном Кавказе она несколько выше.В степной зоне
при повышении засушливости климата действие азотных удобрений уменьшается либо становится очень неустойчивым. Но в условиях орошения эффективность действия азотных удобрений возрастает и бывает даже более высокой, чем фосфорных и калийных удобрений.Типичные черноземы
Молдавии отличаются большими прибавками урожая.Обыкновенные и карбонатные черноземы
Молдавии характеризуются меньшей эффективностью однокомпонентных азотных удобрений.Обыкновенные черноземы
степных районов Украины . Азотные удобрения показывают значительную эффективность, но и действие значительно ослабляется с запада на восток.Обыкновенные и карбонатные черноземы Кубани, предгорий Северного Кавказа, североприазовские черноземы
отличаются значительным положительным действием азотных удобрений.Карбонатные черноземы Ростовской области, обыкновенные черноземы Поволжья
. Эффективность удобрений снижается.Каштановые почвы
. При лучших условиях увлажнения отмечается хорошее действие удобрений. В засушливых условиях действие азотных удобрений бывает слабым.Влияние на сельскохозяйственные культуры
Азотным удобрениям принадлежит ведущая роль в повышении урожайности различных сельскохозяйственных культур. Это связано с ролью азота как важного биологического элемента, играющего исключительную роль в жизни растений.
Достаточное снабжение азотом усиливает синтез органических азотистых веществ. У растений образуются мощные листья и стебли, интенсивность зеленой окраски усиливается. Растения хорошо растут и кустятся, улучшается формирование и развитие органов плодоношения. Эти процессы способствуют повышению урожайности и содержанию белка.
Однако необходимо учитывать, что односторонний избыток азота может задерживать созревание растений, способствуя развитию вегетативной массы при уменьшении развития зерна, корнеплодов или клубней. У льна, зерновых и некоторых других культур избыток азота вызывает полегание (фото) и ухудшение качества растениеводческой продукции.
Так, в клубнях картофеля может снизиться содержание крахмала. В корнеплодах сахарной свеклы снижается сахаристость и возрастает содержание небелкового азота.
При избытке азотных удобрений в кормах и овощах накапливаются потенциально опасные для здоровья человека и животных нитраты.
Получение азотных удобрений
Производство азотных удобрений основывается на получении синтетического аммиака из молекулярного азота и водорода.
Азот образуется при прохождении воздуха через генератор с горящим коксом.
Источники водорода - природный газ, нефтяные или коксовые газы.
Из смеси азота и водорода (соотношение 1: 3) при высокой температуре и давлении и в присутствии катализатора образуется аммиак:
N 2 + 3H 2 → 2NH 2
Синтетический аммиак идет на производство аммонийных азотных удобрений и азотной кислоты, которая используется для получения аммонийно-нитратных и нитратных удобрений.
4.Ягодин Б.А., Жуков Ю.П., Кобзаренко В.И. Агрохимия / Под редакцией Б.А. Ягодина.- М.: Колос, 2002.- 584 с.: ил (Учебники и учебные пособия для студентов высших учебных заведений).
Изображения (переработаны):
5. 6. Свернуть